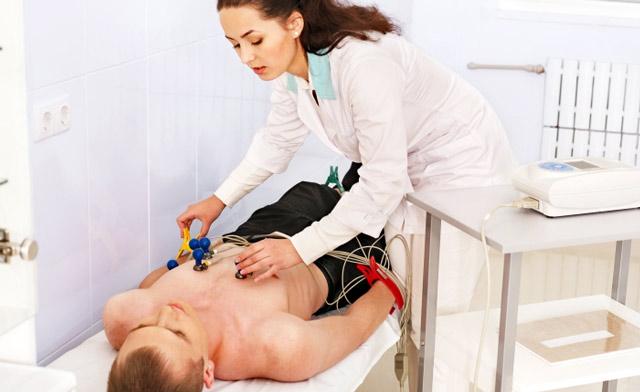
Состояние новорожденных в реанимации может быть крайне сложным и требует внимательного наблюдения и профессионального вмешательства. Стабильно тяжелое состояние подразумевает, что несмотря на осуществляемые меры, ребенок продолжает оставаться в критическом состоянии, что может быть вызвано различными патологиями или осложнениями, возникшими сразу после рождения.
В таких случаях необходимо оперативно адаптировать стратегии лечения, чтобы минимизировать риски и улучшить прогноз. Комплексный подход, включающий мультидисциплинарную команду специалистов, играет решающую роль в поддержании жизненно важных функций и создании условий для возможного восстановления здоровья новорожденных.
- Обсуждается актуальность проблемы стабильного тяжелого состояния новорожденных в реанимации.
- Выделены основные причины, приводящие к тяжелым состояниям у новорожденных, включая родовые травмы и инфекции.
- Подробно рассмотрены методы мониторинга и оценки состояния пациентов в реанимации.
- Приведены примеры клинических случаев и обоснованы подходы к лечению и поддержке новорожденных.
- Оценены перспективы лечения и реабилитации в условиях реанимации для улучшения прогнозов.
Как наблюдают за детьми в отделение реанимации недоношенных. Контроль за состоянием маленьких пациентов ведется круглосуточно
Плоды прогресса
В период до середины 70-х годов медицинские работники были обязаны оказывать помощь только тем новорождённым, которые появились на свет не раньше 28-й недели беременности и weighed хотя бы 1000 граммов. Однако в 1975 году Всемирная организация здравоохранения взглянула на этот вопрос иначе и рекомендовала считать жизнеспособными младенцев, рожденных с 22-й недели и массой от 500 граммов. Россия приняла рекомендации ВОЗ начиная с 1 января 1993 года, но в таких крупных городах как Москва и Санкт-Петербург уже тогда существовали учреждения, где врачи старались справляться с подобными случаями.
Но подходили они к ней в основном с научной, исследовательской, точки зрения. За прошедшие десять лет мы обучили персонал, освоили специальную аппаратуру и лабораторные приборы. Ничего нового для выхаживания глубоконедоношенных детей придумывать нам не приходится, мы стараемся брать готовые технологии и пользоваться опытом западных коллег, у которых в этом вопросе больше практических знаний. К примеру, в 1999 году в США выпустили аппарат «Миллениум», он специально предназначен для искусственной вентиляции легких маловесных детей. Через полгода он был уже в нашем распоряжении (его помог приобрести клинике Внешэкономбанк).
Уход за недоношенными детьми представляет собой похожий процесс на создание оптимальных условий для космонавта в длительном путешествии. Очень важно поддерживать определённые параметры температуры и влажности в окружающей среде. Для этого используются кроватки-кувезы, которые защищают кроху со всех сторон и имеют двойные прозрачные стенки, а также дополнительные источники обогрева. Температура внутри кувеза (36-37°C) устанавливается врачом с учётом индивидуальных особенностей грудничка и должна поддерживаться с высокой точностью, так как даже незначительное колебание в один градус может значительно отразиться на состоянии здоровья и жизни ребенка.
На тело младенца накладываются датчики, которые фиксируют важнейшие параметры: пульс, дыхание, артериальное давление и уровень кислорода. Это делается для того, чтобы не тревожить ребенка лишний раз. Все данные отображаются на экране, и вмешательство медицинского персонала происходит лишь в случае отклонения от норм показателей.
У большинства новорожденных с низким весом легкие недоразвиты и нуждаются в длительной вспомогательной вентиляции. Мы обычно используем аппараты, которые не только поддерживают дыхательные движения, но и стимулируют их, если они слабые.
Важным аспектом является питание. В первые дни жизни подросший желудок способен усвоить лишь несколько миллилитров молока, поэтому питательные вещества вводятся непосредственно в кровеносную систему с помощью тонких трубочек.
Одним словом, тот путь развития, который ребенок должен был пройти в утробе матери, мы помогаем ему осуществить искусственным образом, попутно устраняя факторы, которые препятствуют его внеутробному развитию. Если кроха родился в возрасте 22 недель, он еще по меньшей мере 14-18 недель нуждается в выхаживании. А если он болеет, процесс лечения может затянуться на многие месяцы. Наиболее уязвимым у таких детей является головной мозг. К сожалению, нам далеко не всегда удается спасти им жизнь.
Состояние новорожденных в реанимации нередко характеризуется как стабильно тяжелое. Это означает, что, несмотря на проводимые мероприятия и назначенное лечение, состояние ребенка остается критическим и требует постоянно высокой квалификации медицинского персонала. В таких случаях необходимо внимательно отслеживать не только физическое состояние, но и психоэмоциональное окружение, в котором находится младенец.
Применение высоких технологий, таких как искусственная вентиляция легких и мониторинг жизненно важных показателей, позволяет врачу осуществлять эффективный контроль за состоянием пациента. Однако даже с учетом всех современных методов лечения нельзя исключать вероятность ухудшения состояния, что требует от медиков готовности к быстрому реагированию на любые изменения. Важно, чтобы команда реаниматологов оставалась сплоченной и могла оперативно реагировать на нестандартные ситуации, так как на кону может оказаться жизнь новорожденного.
Кроме этого, следует помнить о важности междисциплинарного подхода в таких сложных случаях. Взаимодействие педиатров, неонатологов и других специалистов, а также поддержка семьи, играют решающую роль в лечении. Как реаниматолог, я понимаю, что создание оптимальных условий для восстановления пациента включает не только эффективную медицинскую помощь, но и создание атмосферы, способствующей его психологическому комфорту, что в свою очередь может позитивно сказаться на динамике выздоровления.
Состояние стабильно тяжелое в реанимации у новорожденных

Сложно дать объективную оценку тяжести состояния новорожденного. Это обусловлено анатомическими и физиологическими характеристиками детей разных сроков гестации, наличием временных состояний и компенсаторных возможностей в зависимости от пренатального развития. Субъективный фактор Вносит немалую долю неопределённости в оценку состояния, поскольку на это влияют специализация, опыт и стаж врача, осматривающего младенца.
В медицине классифицируют состояния пациентов как удовлетворительные, средней степени тяжести, тяжёлые и критические. По общепринятой терминологии, состояние считается удовлетворительным, если «функции жизненно важных органов относительно компенсированы», что обычно наблюдается при лёгких формах заболевания. Однако возникает вопрос: может ли даже легкое течение патологии у новорождённого считаться удовлетворительным состоянием?
Об общем состоянии средней тяжести говорят в случае, «если заболевание приводит к декомпенсации функций жизненно важных органов, однако не представляет непосредственной опасности для жизни больного». Видели ли вы новорожденного ребенка с декомпенсацией хотя бы одной витальной функции, чтобы это не представляло опасности для его жизни?
О состоянии пациента говорят, что оно тяжёлое, когда возникшая в результате заболевания декомпенсация жизненно важных функций представляет угрозу для жизни или потенциально может привести к инвалидности. Учитывая это, неонатологи могут оценивать состояние младенца как критическое, если оно «…характеризуется серьёзными нарушениями основных жизненно важных функций организма и требует срочных мер для спасения».
Таким образом, неонатологи склонны преувеличивать степень тяжести своих пациентов? Да, потому что мы знаем, что состояние ребенка может быстро ухудшаться, и недооценка тяжести может сыграть фатальную роль.
Попытки объективизировать, создать количественную оценку тяжести состояния больных предпринимаются уже более полувека. Шкалы оценки тяжести, используемые в неонатологии:
- PIM II — Индекс смертности у детей, получающих интенсивную терапию (Slater A. и др., 2003);
- PRISM III — Индекс риска смертности у детей (Pollack M.M. и др., 1996);
- SNAP — Балл для неонатальной остропатологии (1993 O.K.Richardson и др.);
- SNAPPE — Балл для неонатальной остропатологии и перинатальная расширенная оценка (R.C. Silveria и др., 2001);
- CRIB — Клинический риск для новорождённых (2000, 2003 G.Pany и др.);
- NEOMOD — Оценка неонатальной множественной органной дисфункции (Janota J. и др., 2001);
Следует отметить, что эти шкалы обладают высокой валидностью, однако они в основном дают краткосрочный прогноз летальности в условиях ОРИТН. Одним из значительных недостатков этих шкал является их неспособность учитывать влияние интенсивной терапии на тяжесть патологии. Ни одна из существующих шкал не позволяет откровенно ответить на вопрос о тяжести состояния конкретного пациента при осмотре.
Исключение составляют шкалы NTISS — Система оценки неонатальных терапевтических вмешательств (Gray J.E., Richardson D.K. и др., 1992), которые измеряют тяжесть состояния на основании объёма и сложности необходимых процедур по уходу. Использование этой шкалы требует строгого соблюдения клинических протоколов и стандартов, что иногда неосуществимо из-за различий в уровне предоставления медицинской помощи.
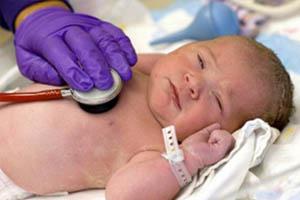
Несмотря на это, неонатологические шкалы оценки тяжести являются полезным инструментом для сравнительной оценки риска неблагоприятных исходов и могут помочь в выявлении потенциальных лучших практик. Как показывает практика, «летальность более точно определяется не весом и гестационным возрастом, а тяжестью состояния пациента, что можно оценить стандартизированными шкалами». Кроме того, объективизация тяжести состояния позволяет корректно планировать маршрутизацию пациентов, расставлять приоритеты в кадровых и технических ресурсах медучреждений.
Практически описание осмотра пациента должно начинаться с оценки общего состояния. Можно ли данную оценку сделать объективной? Возвращаясь к академическому определению, тяжесть состояния пациента определяется степенью функциональной недостаточности систем жизнеобеспечения, т. е. тяжестью течения болезни. Для объективной оценки тяжести состояния используются клинические классификации нозологических форм и ранговые шкалы количественной оценки функциональной недостаточности той или иной системы организма.
В условном порядке выделяют пять систем поддержания жизнедеятельности.
- Дыхательная система.Тяжесть дыхательной недостаточности у новорожденных определяют по шкалам Silverman–Anderson (1956 г.) и Downes (в модификации 1970 г.);
- Сердечно-сосудистая система.Степень тяжести нарушения кровообращения у новорожденных определяют по шкале А. С. Шарыкина (2000 г.) или можно использовать менее известную шкалу R.D. Ross et al (1992 г.) в модификации НЦССХ им. Бакулева;
- Центральная нервная система.Оценка церебральной недостаточности производится с использованием неонатальных шкал комы Глазго/Санкт-Петербург (2005 г.) или Раймонди A.J., Hirschane J. (1984 г.). Степень тяжести церебральной ишемии можно определить по классификации H.B. Sarnat и M.S. Sarnat (1976 г.);
- Желудочно-кишечный тракт. Основной критерий тяжести кишечной недостаточности — это толерантность к энтеральному питанию;
- Мочевыделительная система.Тяжесть острых заболеваний почек у новорожденных оценивается с помощью неонатальной шкалы AKIN (2011 г.) или nRIFLE (2013 г.).
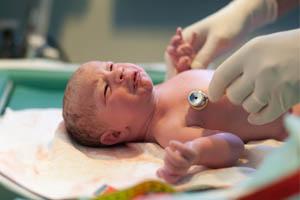
Об оценке состояния детей с хирургической патологией очень хорошо сказал H. Selye (1950 г.) «… критические состояния прооперированных больных определяются самой операцией в не меньшей степени, чем недостаточностью любой функциональной системы. К тому же последствия такой мощной агрессии, как хирургическое вмешательство, всегда сказываются на всем организме».
Существует несколько специфических нозологий перинатального периода, способных влиять на тяжесть состояния новорожденных. К примеру, асфиксия новорожденного. С 1952 года педиатры и неонатологи по всему миру применяют шкалу Апгар для оценки состояния новорождённого в первые минуты его жизни, которая лежит в основании скрининга тяжести асфиксии.
Степень тяжести состояния новорожденного может быть также связана с протекающей гемолитической болезнью; основные критерии определяются клинико-лабораторными данными в соответствии с рекомендациями РОН и РАСПМ (2017 г.).
Необходимо понимать, что в случаях заболеваний страдает не только один орган, но и весь организм в целом, однако даже при множественной органной недостаточности можно выделить основной патологический синдром, который будет определять серьёзность состояния пациента.
Итак, попробуем дать определения тяжести состояния новорожденного ребенка.
Состояние может считаться удовлетворительным, если отсутствуют нарушения функциональности жизненно важных органов. Это касается транзиторных состояний новорождённости, недоношенности, а также детей с задержкой массы и роста или малыми аномалиями развития (при отсутствии нарушения функции органа).
Состояние средней степени тяжести отмечается, когда функциональная недостаточность систему обеспечивается механизмами саморегуляции организма.
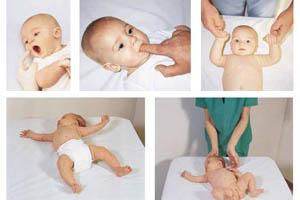
К критериям тяжелого состояния относятся:
- Декомпенсация функций жизненно важных органов
- Полиорганная недостаточность
- Риск летального исхода или инвалидности
- Эффективность интенсивной терапии.
Разница в степени тяжести состояния между тяжелым и критическим заключается в том, что последнее относится к патологическому процессу, при котором более двух основных функций организма не выполняются, и состояние ухудшается, несмотря на проводимое лечение. Таким образом, задача создания интегративных шкал оценки тяжести состояния новорожденных остается актуальной. В практике основным критерием тяжести состояния является степень выраженности ведущего патологического синдрома. Необходимо учитывать, что степень тяжести состояния — это изменчивый показатель, который следует оценивать динамично.
Применение аппарата ИВЛ
Применение аппарата искусственной вентиляции легких становится обязательным, если после выполнения первого этапа ситуация ребенка не улучшилась. Если наблюдается поверхностное дыхание, выраженная бледность кожи, а пульс составляет менее 100 ударов в минуту, переходит ко второму этапу.
Продолжительность второго этапа реанимации не превышает 30 секунд. По прошествии данного времени необходимо оценить состояние младенца. Мероприятия прекращают, если сердечная мышца сокращается со скоростью 100 ударов в минуту и более, а также стабилизируется дыхание и появляется двигательная активность. Если ЧСС не превышает 80, переходят к следующему шагу.
Сердечно-легочная реанимация
На третьем этапе реанимационных мероприятий применяются более продвинутые методы в борьбе за жизнь. Действия медицинских работников сосредоточены на восстановлении сердечной активности и поддержании нормального гемодинамического состояния.

Этапы реанимации четко определены
Алгоритм действий для врача:
- большой палец одной руки помещается на другую в области мечевидного отростка;
- кисти рук обхватывают тело младенца и располагаются за спиной малыша;
- массаж сердца осуществляется с частотой два сжатия в секунду на глубину до 2 см.
Вместе с массажем сердца продолжается легочная реанимация. На три нажатия выполняется один вдох аппаратом со 100% кислородом. Продолжительность данного этапа составляет 60 секунд. При видимых улучшениях состояния массаж сердца прекращают, а ИВЛ оставляют до стабилизации самостоятельного дыхания.
Если в течение минуты после начала сердечно-легочной реанимации состояние младенца остается без изменений, врачи принимают решение о необходимости медикаментозной терапии.
Оценка тяжести состояния новорожденных в отделении реанимации
Объективная оценка тяжести состояния реанимационного пациента важна не только для прогнозирования и определения риска летального исхода, но также для улучшения интенсивной терапии. При этом современные версии известных шкал (например, АРРАСНЕ III, SAPS II, SOFA) не всегда подходят для новорожденных, поскольку они базируются на оценке функциональных нарушений, использующих множество показателей, часто недоступных в неонатальный период (в частности, параметры оксигенации крови) или шкалу комы Глазго.
С целью разработки практически приемлемой шкалы оценки тяжести состояния проанализированы данные обследования 130 новорожденных с хирургической патологией (в основном, с тяжелыми пороками развития — атрезия пищевода, диафрагмальная грыжа, кишечная непроходимость и др.) и перинатальной инфекцией, находившихся на лечении в ОРИТ за последние 5 лет. Исследовано 49 случаев умерших детей и 81 выживших. Тяжесть состояния оценивали в динамике на трех этапах — при поступлении (1-й этап), на 3-5 сутки (2-й этап) и на 10-20 сутки жизни (3-й этап).
В результате проведенного анализа разработана шкала тяжести состояния, включающая оценку пяти органных систем (дыхательной, сердечно-сосудистой, мочевыделительной, желудочно-кишечной и центральной нервной системы). Каждая система оценивалась по клиническим критериям в пределах от 1 до 3 баллов. Затем баллы суммировались, и при сумме 3-5 состояние ребенка расценивалось как тяжелое, 8-10 – очень тяжелое, более 12 – крайне тяжелое.
Учитывая возможность субъективности балльной оценки, ее дополняли общепринятыми показателями, такими как температура тела, состав периферической крови (лейкоцитоз/лейкопения, нейтрофилез/нейтропения, факторы сдвига лейкоцитарной формулы влево, повышенный нейтрофильный индекс, показатели лимфоцитов и моноцитов) и кислотно-щелочное состояние крови (КЩС).
В первые сутки жизни, то есть при поступлении, у выживших новорожденных тяжелое состояние выявлено у 56% детей, очень тяжелое — у 33% и только 11% больных поступало в крайне тяжелом состоянии. В группе умерших соответственно выявлено 24%, 49% и 27%. На 2-м этапе обследования в группе выживших детей у 53% состояние расценено как очень тяжелое и у 13% — как крайне тяжелое; в группе умерших у 67% — очень тяжелое, у 22% — крайне тяжелое. На третьем этапе процент больных в очень и крайне тяжелом состоянии преобладал в группе умерших больных.
Собранные данные позволили установить прямую связь между тяжестью состояния и симптомами системной воспалительной реакции, а также с изменениями КЩС. Была зафиксирована обратная зависимость между сроком гестации и уровнем летальности. Реакция периферической крови не всегда совпадала с уровнем тяжести.
Например, в гемограммах новорожденных с врожденными аномалиями в первые сутки жизни более чем у половины пациентов был отмечен нейтрофилез, тогда как повышение уровня лейкоцитов наблюдалось только у 9,5% новорожденных, лейкопения — у 4% выживших и у 14,2% умерших. На третьи-пятые сутки жизни незначительные изменения лейкоцитов были выявлены у одной трети ребят, в то время как увеличение нейтрофилов сохранялось у всех групп пациентов, лимфопения была отмечена у примерно 70% случаев, проявлялся моноцитоз. На десятые-двадцатые сутки жизни у детей с послеоперационными осложнениями уровень лейкоцитов и нейтрофилов возрос более чем у 85% пациентов; лимфопения продолжала наблюдаться, и у половины детей также проявлялся моноцитоз, среди умерших детей только у 15% было отмечено увеличение моноцитов.
Данное исследование выявило, что тяжесть состояния определяется не столько клинической формой заболевания, сколько наличием полиорганной недостаточности и системной воспалительной реакции вместе со специфической инфекцией. Можно предположить, что предлагаемая шкала оценки тяжести состояния новорожденных, не претендуя на универсальность, будет удобной для практических врачей и найдет применение в неонатальных отделениях и в реанимации.
Диагностика
Диагностировать асфиксию в период вынашивания плода (первичную, или внутриутробную) позволяют:
- мониторинг сердечного ритма плода, выполняемый во время кардиотокографии;
- оценка двигательной активности, дыхания и тонуса мышц плода с применением ультразвукового исследования.
При вторичной асфиксии, возникающей внеутробно, диагноз выставляется с учетом наличия симптомов патологического состояния, общего состояния младенца, степени выраженности кислородного голодания и последующих анализов, проводимых после выполнения алгоритма неотложной помощи.
Для диагностики применяются:
- оценка по шкале Апгар;
- анализ крови, взятой из головы, сосудов пуповины плода, с определением уровня кислорода, углекислого газа и кислотности.
В некоторых случаях также назначают ультразвуковое исследование головного мозга, с помощью которого определяют, насколько поражена центральная нервная система. Обследование также позволяет отличить гипоксическое повреждение нервной системы от травматического.
Лечение
Клинические рекомендации по действию при асфиксии акцентируют внимание на первоочередной необходимости оказания помощи новорожденному. Это критически важный этап, который при правильной организации помогает минимизировать последствия и снизить риск осложнений. Основная цель реанимации при асфиксии – добиться наивысшего результата по шкале Апгар в интервале 5-20 минут после рождения.
Эффективная и последовательная реанимация новорожденного, столкнувшегося с асфиксией, осуществляется в соответствии с этапами и принципами АВС-реанимации. Источник:
Проведение лечебной гипотермии у новорожденных, родившихся в асфиксии. К. Б. Жубанышева, З. Д. Бейсембаева, Р. А. Майкупова, Т. Ш. Мустафазаде. Наука о жизни и здоровье, 2019. с. 60-67 :
- Принцип A («airway») – обеспечить проходимость дыхательных путей на первичном этапе реанимации. Для этого следует правильно расположить голову: запрокинуть ее и наклонить вниз на 15 градусов. Затем отососать слизь и околоплодные воды из носа, рта, трахеи и нижних отделов дыхательных путей.
- Принцип B («breath») – создать вентиляцию и обеспечить дыхание. Для этого используется кислородный поток с проведением искусственной вентиляции легких с помощью реанимационного мешка. Если младенец не плачет, необходимо добавить тактильную стимуляцию: поглаживание по спине и похлопывания по стопам.
- Принцип C («cordial») – восстановить сердечную функцию. Для этого применяется непрямой массаж сердца. При необходимости вводится адреналин, глюкоза, гидрокортизон и другие медикаменты, при этом нельзя приостанавливать вспомогательную вентиляцию.
План последующего лечения и ухода определяет лечащий врач. Общие рекомендации по уходу включают:
- поддержание нормальной температуры тела, артериального давления и частоты сердечных сокращений;
- обеспечение комфорта: оптимальная температура окружающей среды и удобное положение;
- проведение дыхательной терапии;
- инфузионная терапия – введение жидкости для удовлетворения потребностей.
В процессе реабилитации поддерживать контроль за состоянием ребенка помогает регулярный мониторинг:
- веса малыша (два раза в день);
- неврологического и соматического состояния;
- объема потребляемой жидкости;
- питательного состава;
- основных жизненных показателей: пульса, артериального давления, уровня сатурации, частоты дыхательных движений;
- лабораторных показателей крови и мочи;
- рентгеновских снимков грудной клетки и живота;
- ультразвукового обследования живота;
- нейросонографии;
- электрокардиограммы и эхокардиограммы.
После выписки малыша нужно регулярно наблюдать у педиатра, невропатолога.
Кому задавать вопросы о состоянии ребенка
Двери отделения реанимации открываются санитарками, медсестрами или лаборантами. Не имеет смысла задавать им вопросы о состоянии младенца, так как у них нет права на ответ. Ожидайте врача.
Уход за детьми в реанимации осуществляют анестезиологи или реаниматологи. Это разные названия одной и той же специальности. За каждым пациентом в ОРИТ закреплен врач из соответствующего отделения. Анестезиологи-реаниматологи находятся рядом с ребенком круглосуточно, тогда как врачи профильного отделения навещают его один или несколько раз в день.
Пока ребенок лежит в реанимации, общайтесь с врачами из этого отделения. В рабочее время это может быть заведующий отделением или лечащий анестезиолог. В выходные и праздники на вопросы ответит дежурный анестезиолог. Врачи в ОРИТ присутствуют круглосуточно.
Легкий способ отличить врача от медсестры или санитара — взглянуть на бейдж. Да, это очевидно, но в ОРИТ можно забыть даже об этом.
Что спросить у врача
Не стесняйтесь задавать вопросы о здоровье ребенка. Врач – это единственный специалист, имеющий полные данные о состоянии пациентов в реанимации и способный обсудить эту информацию с родителями. Обычно специалисты стараются общаться без сложных терминов. Однако, если в беседе что-то останется непонятным, обязательно переспросите и попросите разъяснения.
Во время разговора врач может оценить состояние пациента по степени тяжести. Вот что это значит.
- Состояние удовлетворительное. Ключевые органы функционируют без отклонений. При таком состоянии дети попадают в реанимацию исключительно для наблюдения, например, после поражения электрическим током, даже если они хорошо себя чувствуют.
- Состояние средней тяжести. Функциональные нарушения в важных органах присутствуют, но прямо сейчас жизнь ребенка не в опасности. Он останется в реанимации до улучшения состояния.
- Тяжелое состояние. Наблюдаются серьезные нарушения работы жизненно важных органов, имеется угроза для жизни пациента.
- Стабильно тяжелое состояние. Состояние ребенка существенно не меняется, то есть улучшения или ухудшения не наблюдаются.
- Крайне тяжелое состояние. Существуют резкие нарушения функций ключевых органов, есть острая угроза для жизни ребенка; требуется интенсивная терапия.
- Агональное или фатальное состояние. Ситуация крайне серьезная. Пациент на грани смерти — его жизнь может оборваться в течение нескольких минут или часов. Также этот термин часто используется для обозначения умирающих людей, которые больше не могут быть спасены врачами.
Когда медицинский работник сообщит о здоровье вашего ребенка, уточните, как вы можете оказать помощь. Задавайте конкретные вопросы, чтобы получить ясные указания, например: «Что именно нам нужно сделать прямо сейчас?»
Если вы можете внести свой вклад, врач обязательно об этом скажет. Например:
- Приобрести или организовать доставку медикаментов. Хотя экстренная и неотложная помощь по закону предоставляется бесплатно, в отделении интенсивной терапии могут отсутствовать редкие или специализированные препараты, необходимые вашему ребенку.
- Сдать кровь. Практически все маленькие пациенты в реанимации нуждаются в переливании крови, поэтому врачам важно, чтобы родственники пациентов сдавали кровь.
- Привести молоко, если в реанимацию попал новорожденный. Мать может сцеживать молоко и передавать его врачам.
- Оказать помощь в уходе за ребенком.
Старайтесь избегать вопросов о прогнозах. Врач оценивает состояние пациента, исходя из текущей ситуации, которая может меняться в любую сторону за считанные минуты или часы. После медицинских манипуляций состояние может улучшиться — смениться с критического на тяжелое или среднее. К сожалению, бывает и обратное.
Из-за этого многие врачи не любят давать прогнозы и отвечают дежурными фразами на вопросы, которые больше всего волнуют родителей. Страшное исключение из этого правила: если шансов на благополучный исход нет, врачи прямо говорят об этом родственникам больного.
Опыт других людей
Алексей, 32 года: «Когда моя дочь родилась, врачи сразу сказали, что состояние стабильно тяжелое. Эти слова заставляли моё сердце замирать. В реанимации нам сказали, что у неё проблемы с дыханием и что они будут делать всё возможное. Я помню, как каждую минуту следил за мониторами, надеясь увидеть какие-то улучшения. Это было очень тяжело, но поддержка близких помогала мне пережить этот ужас.»
Екатерина, 28 лет: «Мой сын появился на свет раньше срока и сразу попал в реанимацию. Врачи объяснили, что его состояние стабильно тяжелое, и нам нужно набраться терпения. Каждый день я приходила в больницу, и мне было страшно видеть его в инкубаторе. Я молилась за него, hoping for miracles and watching how the nurses cared for him. Это была самая трудная неделя в моей жизни.»
Сергей, 40 лет: «Когда наш малыш оказался в реанимации, мы испытали настоящий шок. Врачи сказали, что его состояние стабильно тяжелое, что это может быть связано с множеством факторов. Я часто думал о том, что значит быть родителем, когда твой ребёнок так маленький и слабый. Мы пытались быть оптимистами, хотя это было невероятно сложно. Каждый шаг к выздоровлению давал нам надежду.»
Вопросы по теме
Каковы основные причины тяжелого состояния новорожденных в реанимации?
Основные причины тяжелого состояния новорожденных в реанимации включают дыхательную недостаточность, инфекционные заболевания, асфиксией при родах, недоношенность, а также различные генетические и метаболические расстройства. Каждая из этих причин может привести к серьезным нарушениям, требующим интенсивного медицинского вмешательства и постоянного мониторинга.
Какие меры можно предпринять для улучшения состояния новорожденных в реанимации?
Для улучшения состояния новорожденных в реанимации важно следовать ряду ключевых мер. В первую очередь, необходима установка стабильного дыхания с помощью вентиляции, поддержка нормальной температуры тела и адекватное увлажнение. Также важна педиатрическая оценка, включающая использование медикаментов для коррекции жизненно важных функций и, при необходимости, проведение оперативных вмешательств. Кроме того, психологическая поддержка для родителей играет огромную роль в процессе выздоровления.
Каковы прогнозы и долгосрочные последствия для детей, перенесших тяжелое состояние в реанимации?
Прогнозы для новорожденных, перенесших тяжелое состояние в реанимации, зависят от ряда факторов, включая возраст ребенка, наличие сопутствующих заболеваний и длительность лечения. Некоторые дети могут полностью восстановиться и не испытывать долгосрочных последствий, в то время как другие могут столкнуться с неврологическими или развитием физическими нарушениями. Регулярное наблюдение и реабилитация необходимо для оценки развития и коррекции возможных отклонений.